서 론
재료 및 방법
생물학적 특성 검정
바이러스 검정 및 염기서열 결정
유전적 상동성 분석
결과 및 고찰
CMV-Sp의 생물학적 반응
CMV-Sp의 전체 염기서열과 비교 분석
CMV-Sp의 고추에서의 생물학적 특성 분석
요 약
서 론
예루살렘 체리(Solanum pseudocapsicum)는 남아메리카가 원산지인 가지과에 속하는 다년생 낙엽관목으로 국내에는 관상용으로 수입 유통된다. 국내에서 예루살렘 체리는 윈터 체리, 옥천 앵두 등으로 불린다. 예루살렘 체리는 Cucumber mosaic virus (CMV)를 비롯하여, Tomato spotted wilt virus (TSWV), Paprika mild mottle virus (PaMMV), Pepper leaf curl Lahore virus (PepLCLV), Eggplant mottled crinkle virus (EMCV) 등 다양한 바이러스가 감염하는 것으로 알려져 있으며 국내에선 최근 CMV가 처음으로 보고되었다(Smith, 1931; Tobias et al., 1982; Camele et al., 1986; Raj et al., 1989; Srivastava et al., 2013; Park et al., 2018).
CMV는 100개과 1200여종의 매우 넓은 기주범위를 가지고 있는 바이러스로 3개의 분절게놈과 2개의 서브게놈을 가지고 있다(Palukaitis and Garcia-Árenal, 2003; Mochizuki and Ohki, 2012). 또한, 진딧물에 의해 비영속적으로 전염되는 특성을 가진다(Palukaitis and Garcia-Árenal, 2003; Kim et al., 2012). 또한, CMV 분리주들은 분리 기주와 바이러스의 유전적 차이에 의해 분리주 간 감염 기주에 차이가 있는 것으로 알려져 있다. 따라서 본 연구에서는 예루살렘 체리로부터 분리된 CMV 분리주, CMV-Sp에 대해 전체 염기서열을 결정하고 다른 CMV 분리주와 비교하였으며 다양한 고추품종에서의 생물학적 특성을 분석하였다.
재료 및 방법
생물학적 특성 검정
바이러스의 생물학적 특성을 분석하기 위해 바이러스에 감염된 잎을 0.01 M 인산완충용액과 함께 마쇄한 뒤, 가지과(Solanaceae), 명아주과(Chenopodiaceae), 박과(Cucurbitaceae), 콩과(Fabaceae), 꿀풀과(Lamiaceae)에 속하는 식물 10종(Nicotiana benthaminana, N. rustica, N. tabacum cv. Xanthi nc, N. tabacum cv. Samsun, Capsicum annuum, Chenopodium quinoa, C. amaranticolor, Cucurbita pepo cv. Choigobong, Cucumis sativus, Vigna unguiculata, Perilla frutescens var. japonica)을 대상으로 지표식물에 즙액 접종하였다. 접종 14일 후, 바이러스의 전신감염 여부를 확인하기 위해 접종엽과 상엽에 대해 바이러스 검정을 진행하였다.
바이러스 검정 및 염기서열 결정
바이러스 감염을 확인하기 위해 외피단백질을 포함하는 특이 프라이머(CPT_all for: 5'-YASYTTTDRGGTTCAATTCC-3', CPT_all rev: 5'-GACTGACCATTTAAGCCG-3')를 이용하였다. 바이러스의 RNA는 Phenol-Chloroform RNA 추출 기법으로 추출하였고 M-MLV reverse transcriptase (Promega, USA)를 사용하여 42°C, 1 h 조건으로 cDNA를 합성하였다. 합성된 cDNA는 94°C, 3 min; 35 cycles (94°C, 30 s; 50°C, 30 s; 72°C, 30 s); 72°C, 5 분의 조건으로 PCR 증폭하였다.
CMV-Sp의 전체 염기서열 결정을 위해 전장 염기서열을 증폭할 수 있는 특이 프라이머(RNA1 for: 5'-CGGGATCCTAATACGACTCACTATAGTTTTATTTACAAGAGCGTACG-3', RNA2 for: 5'-CGGGATCCTAATACGACTCACTATAGTTTATTYWCAAGAGCGTA-3', RNA3 for: 5'-CGGGATCCTAATACGACTCACTATAGTAATCTTACACTGTGTGTGTG-3', RNA1, RNA2, RNA3 rev: 5'-AACTGCAGCTGCAGTGGTCTCCTTTTG-3')를 이용하였다. 각 분절게놈의 cDNA는 94°C, 3 min; 35 cycles (94°C, 30 s; 50°C, 30 s; 72°C, 3 min); 72°C, 5 min의 조건으로 PCR 증폭하였다. RT-PCR 산물은 BamHI과 PstI의 제한효소를 이용하여 pUC19 vector (NEB, UK)에 클로닝하였고, CMV-Sp의 전체 염기서열 결정하였다.
유전적 상동성 분석
CMV-Sp에 대한 유전자 분석을 위해 NCBI에 등록된 CMV 염기서열 정보를 수집하였다. 수집 및 CMV-Sp의 1a, 2a, 2b, 이동단백질, 외피단백질 염기서열 정보는 각각 MEGA7 프로그램을 이용해 정렬 및 비교 분석하였다. 2b 단백질은 BioEdit 프로그램을 이용하여 분리주 간 상동성 분석을 실시하였다.
결과 및 고찰
CMV-Sp의 생물학적 반응
예루살렘 체리로부터 순수 분리된 CMV-Sp에 대해 생물학적 특징을 조사하기 위해, 다양한 기주식물에 즙액 접종하여 그 반응을 CMV-Fny를 대조바이러스로 이용해 비교하였다. CMV-Sp는 CMV-Fny와 유사한 감염성을 유도하였으나 오이와 담배에서 CMV-Fny에 비해 강한 병원성을 나타나는 특징이 관찰되었다(Table 1). 고추 품종 부강에서 CMV-Sp는 전신감염 하며 모자이크 병징을 유도하였지만, CMV-Fny는 감염하지 않는 특성이 나타났다(Table 1).
Table 1. Reaction of test plant to CMV-Sp
CMV-Sp의 전체 염기서열과 비교 분석
CMV-Sp의 유전적 특성을 확인하고자 전체 염기서열을 pUC19 vector (NEB, UK)에 클로닝하여 Genbank 등록(Genbank accession No. LC390165, LC390166, LC390167)하고 BLAST 분석을 실시하였다. BLAST 분석 결과, CMV-Sp의 염기서열은 국내 고추에서 분리된 CMV 계통들과 높은 유사성을 나타내었다. CMV-Sp의 특성의 추가적인 분석을 위해 1a 단백질, 2a 단백질, 2b 단백질, 이동 단백질과 외피 단백질의 5가지 ORF를 아미노산 수준에서 CMV 고추 분리주들과 각각 비교하였다. 1a 단백질은 97.8%에서 99.3%의 상동성을 나타냈으며, 2a 단백질은 98.8%에서 99.7%의 상동성을 나타냈다(Table 2). 이동 단백질은 93.2%에서 97.9%의 상동성을 보였으며, 외피 단백질의 96.8%에서 99.7%의 상동성을 보였다(Table 2). 2b 단백질은 96.4%에서 97.3%의 상대적으로 낮은 상동성이 확인되어(Table 2), 아미노산 alignment 분석을 실시하였다. CMV-Sp와 CMV 고추 분리주들은 공통적으로 2b 단백질의 92번째 아미노산인 aspartic acid (D) 하나가 삽입된 돌연변이 형태로 나타났다(Fig. 1). 또한, CMV-Sp의 경우 2b 단백질의 보존된 지역인 22KKQRRR27 Nuclear localization sequences 1 (NLS1) 도메인에서 22KKQKQR27 아미노산으로 변환된 돌연변이를 확인하였다(Fig. 1). 2b 단백질은 식물의 방어기작인 RNA silencing을 억제하는 역할을 하는 것으로 알려져 있으며 특히, lysine (K)과 arginine (R)이 풍부하게 존재하는 NLS1과 NLS2 도메인이 중요하다는 것이 보고되었다(González et al., 2010; Wang et al., 2004). 이전 보고와 마찬가지로 CMV 분리주의 비교분석 결과 2b 단백질의 NLS1과 NLS2 지역은 아미노산이 보존적인 것으로 나타났고, CMV-Sp의 2b 단백질은 NLS2 도메인이 보존된 것으로 확인되었다(Fig. 1). 이들 결과로부터, CMV-Sp와 CMV 고추 분리주 간 유전적 근연관계가 가까운 것으로 확인되었다.
Table 2. Identity (%) of the nucleotide/amino acid sequence of 1a, 2a, 2b, MP and CP between CMV-Sp and other CMV isolates
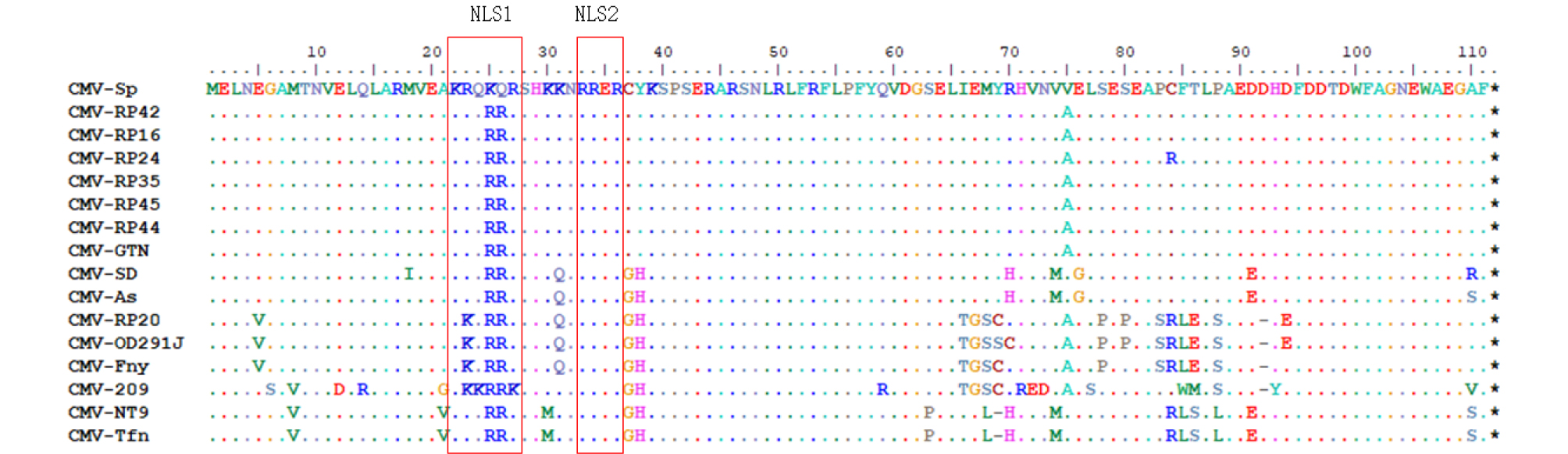
Fig. 1.
2b protein-based multiple sequence alignment of CMV-Sp with other CMV isolates. Identical amino acid sequences have been shown by dots and differences by letters. The dashes represent gaps. Red boxes indicated the nuclear localization sequences (NLS) domain 1 and 2. Nucleotide sequences of the entire genomes were obtained as follows (accession no.) : CMV-SD (D86330), CMV-As (AF033667), CMV-RP20 (KC527704), CMV-OD291J (LC066436), CMV-Fny (D00355), CMV-209 (KJ400003), CMV-NT9 (D28780), CMV-Tfn (Y16925).
CMV-Sp의 고추에서의 생물학적 특성 분석
고추는 국내의 주요 채소작물이며 CMV에 의한 피해가 큰 것으로 알려져 있으며, CMV에 대한 저항성 품종을 개발, 이용해왔으나 저항성을 극복하는 새로운 계통의 CMV가 출현하여 CMV-P0 type과 CMV-P1 type으로 구분하였다(Lee et al., 2006; Kwon et al., 2018). CMV에 대한 저항성 극복에 따른 pathotype의 구분과 CMV-Sp의 생물학적 반응과 유전적 상동성에 기초하여 국내 시판 고추 11품종에 CMV-Sp와 CMV-Fny (P0 type), CMV-CaCh1 (P1-type)을 각각 접종하여 고추의 반응을 비교하였다. 그 결과 P0 type인 CMV-Fny는 천리향, 대들보, 롱그린, 청양 품종에서 모자이크 병징을 유도하였고, PR스마트, PR싹쓸이, PR케이스타, 부강, 배로따, 마니따에 전신감염하지 않는 것으로 확인되었다(Table 3). CMV-Sp는 CMV-CaCh1와 마찬가지로, 천리향, 대들보, 롱그린, 청양과 더불어 PR스마트, PR싹쓸이, PR케이스타, 부강, 배로따, 마니따 등 11품종에 대해 전신 모자이크 병징을 나타내는 CMV-P1 type으로 확인되었다(Table 3). 결과적으로, CMV-Sp는 예루살렘 체리에서 분리된 바이러스로 유전적, 생물학적 특성이 고추에서 분리된 CMV와 유사하다는 것을 확인하였다.
Table 3. Response of pepper cultivars to CMV-Sp
식물 바이러스는 기주식물에 의존적인 생존을 하는 것으로 알려져 있다(Heinlein, 2015). 기존에 예루살렘 체리에서 발견된 CMV, TSWV, PaMMV, PepLCLV 등은 고추에서 자연 발생 하는 것으로 보고되어 예루살렘 체리와 고추에 감염하는 바이러스가 두 식물 모두에 적응할 수 있다는 가능성을 제시한다(De Avila et al., 1991; Hamada et al., 2003; Kim et al., 2014; Tahir et al., 2010). 따라서 CMV-Sp의 저항성 고추에 감염하는 특성은 분리 기주인 예루살렘 체리와 고추가 같은 가지과의 식물로, 가까운 근연관계를 가지기 때문인 것으로 사료된다. 또한, 이러한 사실은 예루살렘 체리 감염 바이러스와 고추 감염 바이러스간의 교차 감염에 대한 가능성을 제시한다.
요 약
예루살렘 체리로부터 Cucumber mosaic virus (CMV)의 한 계통인 CMV-Sp가 분리 동정되었다. CMV-Sp는 CMV-Fny와 지표식물에서 생물학적 특성이 유사하였다. 특히, 고추 품종(부강)에서 CMV-Sp는 전신적인 모자이크 병징을 나타낸 반면에, CMV-Fny는 전신감염 하지 못하는 특성의 차이가 확인되었다. CMV-Sp의 염기서열을 분석하기 위해, 전체 게놈에 대해 염기서열을 결정하고 다른 CMV 분리주들과 비교 분석을 실시하였다. 그 결과, CMV-Sp는 국내 고추에서 분리된 CMV 계통들과 높은 유사성을 가지는 것을 확인하였다. 추가적으로 CMV-Sp의 1a, 2b, 2b, 이동 단백질, 외피 단백질의 유전자를 대상으로 CMV 고추 분리주들과 비교하였다. 1a, 2a, 이동 단백질과 외피 단백질은 각각 98.3%, 98.8%, 93.2%, 96.8% 이상의 높은 상동성을 나타내었다. 또한, CMV-Sp의 2b 단백질의 경우 97.3% 이하의 상동성을 나타내었다. 2b 단백질의 낮은 상동성을 조사하기 위해 2b 단백질 간 아미노산 서열의 비교 분석을 진행하였다. 그 결과, CMV-Sp의 2b 단백질은 보존된 영역인 22KKQRRR27 NLS1의 도메인이 22KKQKQR27으로 바뀐 것을 확인하였다. CMV-Sp의 기주반응과 염기서열 분석을 바탕으로 CMV-Fny (P0 type)과 CMV-CaCh1 (P1 type)과 함께 다양한 고추 품종에서 생물학적 특성을 조사한 결과, CMV-Sp와 CMV-CaCh1는 모든 고추품종에서 전신감염 하였으며, CMV-Fny는 감염하지 못하는 특성을 나타냈다. 이들 결과로부터, 전체 염기서열 분석과 고추에서의 반응을 바탕으로 CMV-Sp는 CMV 고추 분리주들과 매우 유사함을 확인하였다.




