서 론
재료 및 방법
실험재료 및 시약
표준용액 및 시험용액의 조제
Pectolinarin 분석
분석법의 유효성 검증
특이성
직선성
정밀성 및 정확성
검출한계 및 정량한계
결과 및 고찰
Pectolinarin의 분석법 확립
특이성 확인
직선성 확인
정밀성 및 정확성
검출한계 및 정량한계
미세분말 공기분급을 통한 곤드레의 pectolinarin함량 분석
요 약
서 론
생활수준의 향상에 따른 생활리듬 및 식생활의 변화 등에 의해 각종 성인병이 급격하게 증가하고 있다. 이에 따라 건강에 대한 관심이 높아지고 있으며, 암이나 심장병을 포함한 성인병은 식품섭취와 많은 연관성이 있는 것으로 알려져 있다(Kitahara et al., 1992). 건강에 대한 관심이 증대되면서 독특한 향과 맛 때문에 대부분 식용으로 이용되는 청정지역의 산채에 대한 관심도가 증가되고 있으며, 산채에 포함되어 있는 성분의 생리적인 기능이 밝혀짐에 따라 식품 및 약리학적 가치가 새롭게 부각되고 있다. 자연식품을 선호하는 소비패턴의 변화로 산채의 기능적 특성이 알려지면서 농가의 새로운 고부가가치 작목으로 부상하고 있으며, 청정 친환경 식품산업이 급속히 신장됨에 따라 산채도 기능성, 청정성, 안전성을 겸비한 식품으로 알려져 있다(Hwang et al., 2014). 미세분말은 물질 표면적을 최대화하여 용해도를 높여 식품 및 바이오산업에서 활용도가 증진되는 장점을 가지고 있으며, 상대적으로 유용물질의 추출이 용이하고, 색이나 향기 등의 파괴를 줄이는 소재로서, 분말의 분쇄 중 저온을 유지함으로써 색감과 향기를 최대한 유지시켜 주는 장점이 있다(Park et al., 1996). 이와 같은 미세 분말을 활용한 음료의 경우, 목 넘김, 복용 편이성, 건강기능성이 강조됨으로써 판매가 지속적으로 상승하고 있다(Park et al., 1996). 미세 분말화 기술 개발은 용해도 증진을 통해 체내 흡수율을 높이는 기능성 식품소재나 식의약 소재 등 고부가가치 소재로의 전환이 가능 할 것으로 기대된다(Kim et al., 2002; Jung and Lee, 2007).
고려엉겅퀴라고도 불리우는 곤드레(Cirsium setidens)는 해발 700 m 이상의 고지에서 자생하는 국화과의 다년생 초본으로, 맛이 담백하고 부드러워 나물 등의 요리에 사용되는 식재료로 한방에서 염증, 부종, 고혈압 등의 여러 증상에 사용되어 왔다(Lee et al., 2002). 탄수화물의 함량이 높고 리놀렌산, 리놀레산 등의 필수지방산이 함유되어 있으며, 칼륨 등 총 7가지 무기성분이 함유되어 있는 등 다양한 영양성분이 곤드레의 잎 부분에 함유되어 있다(Lee et al., 2006). 뿐만 아니라, 플라보노이드의 일종인 pectolinarin을 비롯하여 luteolin, hispidulin, apigenin 등 여러 종류를 함유하고 있는 것으로 알려져 있어(Thao et al., 2011; Jeong et al., 2008), 곤드레의 생리 활성에 대한 연구가 활발히 진행되고 있다(Lee et al., 2016; Chung et al., 2016; Ahn et al., 2014). 곤드레의 지표성분은 pectolinarin 및 이의 비배당체 형태인 pectolinarigenin으로(Nugroho et al., 2011; Yoo et al., 2008), Lee et al. (2014)의 연구에 따르면 곤드레에 함유된 pectolinalin이 높은 함량을 나타냈다. Cirsium subcoriaceum으로부터 분리된 pectolinarin은 진통과 항염작용이 보고되었고(Martínez-Vázquez et al., 1998), Linaria reflexa Desf에서부터 얻은 pectolinarin에서는 항종양 효과가 있는 것으로 보고되었으며(Tundis et al., 2005), Cirsium japonicum DC 중의 pectolinarin은 항암활성이 보고되었다(Liu et al., 2007; Liu et al., 2006).
이러한 곤드레를 건강기능식품 소재로 개발하는데 함유되어 있는 고유의 성분을 유효 혹은 지표성분으로 설정하고 이에 대한 기준을 확립하여 생산 전반에 걸쳐 일정한 품질이 유지되도록 하는 것이 중요하다. 기능성 원료의 품질이 일정하게 유지되는 것을 확인하기 위해 지표성분을 설정하고 관리하는데, 기준 규격을 설정하기 위해서는 분석법의 타당성 및 신뢰성이 검증되어야 한다. 천연물에 존재하는 지표성분에 대한 기준 및 규격을 설정하기 위해서는 공인된 분석방법 또는 정밀한 분석방법을 사용하여야 하며, 기준 규격의 설정을 위해 분석방법의 타당성 및 신뢰성이 검증되어야 한다(Choi et al., 2017; Kim et al., 2013). 따라서 본 연구에서는 공기분급을 통한 미세분말 곤드레를 건강기능식품 원료로 개발 시 원료의 표준화를 위하여 pectolinarin의 분석방법 및 분석법의 검증에 대한 연구를 실시하였다.
재료 및 방법
실험재료 및 시약
본 연구에서 사용한 건조 곤드레 원료는 ㈜정선약초백화점(Jeongseon, Korea)로부터 구입하였다. 건조 곤드레를 미세분쇄/분급 처리하기 전, 분쇄 효율을 높이고자 MS-200 분쇄기(Myeongseong Co. Ltd, Chengju, Korea)를 사용하여 조분쇄 한 후 열풍건조기로 60°C에서 8시간 재건조를 실시하였다. 건조된 조분쇄물은 Soro-100N 미세분쇄/분급기(Sorobio Co. Ltd, Jeonju, Korea)를 이용하여 3,500-3,800 RPM으로 곤드레 미세분쇄/분급을 실시하여 pectolinarin 고함유 곤드레 분말을 제조하였다. 조분쇄된 곤드레 시료 투입량(각 7.5 kg) 대비 곤드레 분말의 회수량은 1.7 kg(22.7%)으로 나타났다.
표준용액 및 시험용액의 조제
Pectolinarin (Sigma Co., St. Louis, MO, USA) 표준물질 10 mg을 취하여 10 mL 정용플라스크를 이용해 1,000 µg/mL의 농도가 되도록 80% ethanol로 표선까지 정용하여 이를 stock solution으로 하였다. Working solution은 제조된 stock solution을 80% ethanol로 희석하여 0.5, 1, 5, 10, 25, 50, 100 µg/mL가 되도록 하였다. 시험용액은 미세분쇄 된 시료 1 g에 80% ethanol을 10 mL 첨가하고 교반기(SI-600R, JeioTech, Seoul, Korea)로 교반(130 rpm, 30 min)한 후 원심분리기(3,000 rpm, 10 min)를 사용하여 상층액을 취하였으며, 이를 0.45 µm pore size PET syringe filter (Whatman, Maidstone, UK)으로 여과하여 시험용액으로 하였다.
Pectolinarin 분석
곤드레 미세분말의 pectolinarin 함량을 분석하기에 앞서 pectolinarin의 HPLC 분석조건을 확립하였다. Pectolinarin 함량은 다양한 종류의 컬럼을 적용하였을 때 peak가 가장 뛰어난 컬럼을 선정하기 위하여 제조회사가 서로 다른 2종류의 C18컬럼을 대상으로 분석을 실시하였다.
분석법의 유효성 검증
분석법의 유효성 검증은 의약품 등 시험방법 밸리데이션 가이드라인(KFDA, 2018)을 근거로 하여 특이성(specificity), 직선성(linearity), 정밀성(precision), 정확성(accuracy) 및 검출한계(limits of detection, LOD), 정량한계(limits of quantification, LOQ)를 이용하여 분석법의 유효성을 검증하였다.
특이성
표준물질 pectolinarin 및 시료를 HPLC로 분석하여 얻은 chromatogram을 비교하여 pectolinarin의 머무름 시간을 확인하였으며 photodiode-array(PDA) spectrum을 확인하여 동일한 spectrum을 나타내는지 확인하였다.
직선성
Pectolinarin 표준물질을 0.5, 1, 5, 10, 25, 50, 100 µg/mL의 농도로 제조해 HPLC를 이용하여 3회 반복 측정했으며, 각 표준물질의 peak에 대한 면적과 농도비의 관계를 표시하는 검량선을 작성하고 작성한 검량선으로부터 얻어진 상관계수(correlation coefficient, R2) 값을 통해 직선성을 확인하였다.
정밀성 및 정확성
농도를 알고 있는 곤드레 분말 시료에 표준용액 pectolinarin을 10, 25, 50 µg/mL의 농도씩 각각 첨가해 일내(Intra-day) 정밀성 및 정확성을 확인하기 위해 하루에 3회 반복하여 HPLC로 분석하였으며, 일간(Inter-day) 정밀성 및 정확성을 확인하기 위해 3일간 반복하여 HPLC로 분석하였다. 분석하여 얻어진 peak의 머무름 시간(retention time)과 PDA spectrum을 비교하여 정성을 하고 작성한 검량선에 시험용액의 peak 면적을 대입하여 pectolinarin의 농도를 계산하였다. 각 결과 값의 표준편차를 결과 값의 평균으로 나눈 비인 상대표준편차(relative standard deviation, RSD)로 일내 및 일간 정밀성을 확인했으며, 정확성은 다음 식을 이용하여 첨가한 농도에 대비하여 회수된 농도를 계산함으로서 회수율을 구해 정확성을 확인하였다.
% recovery=
Cf : Concentration of spiked sample
Cu : Concentration of sample
Ca : Concentration of standard solution
검출한계 및 정량한계
Pectolinarin의 검출한계(Limit of detection, LOD) 및 정량한계(Limit of quantitation, LOQ)는 검량선의 기울기와 표준편차에 근거하는 방법을 사용했으며 다음 식을 이용하여 확인하였다.
σ: The standard deviation of the response
S : The slope of the calibration curve
결과 및 고찰
Pectolinarin의 분석법 확립
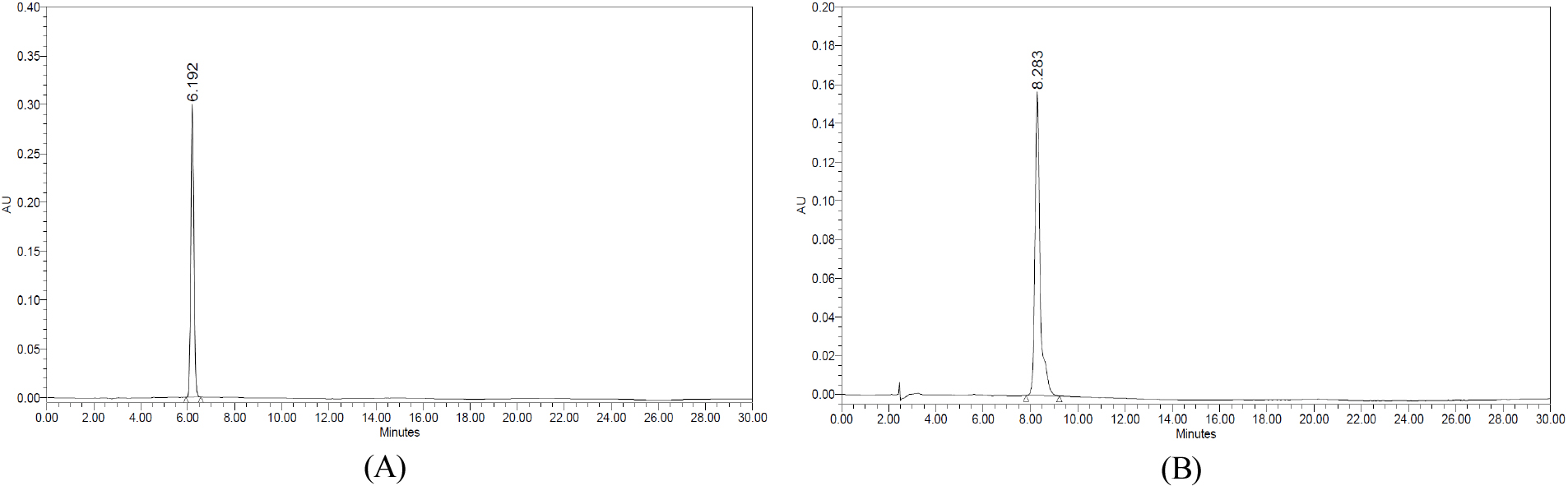
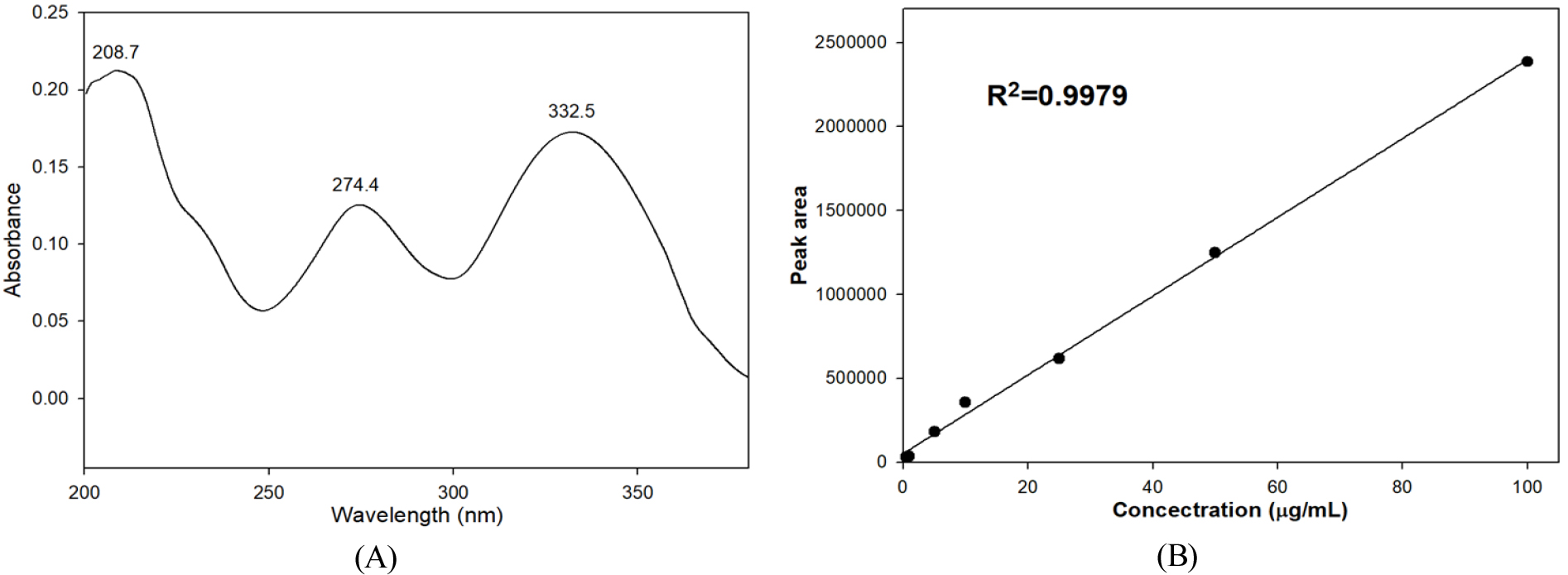
미세분말 곤드레에 함유된 지표성분을 구명하기 위하여 기존의 보고된 분석법을 재현한 결과, 분석시간이 길고 안정화 시간이 짧아 반복 측정 시 기기의 안정화가 제대로 이루어지지 않아 재현성이 낮은 문제점을 보여 기기 조건을 일부 변형하여 최적 분석조건을 확립하였으며(Table 1), 본 실험에서 사용한 컬럼을 비교한 결과는 Fig. 1에 나타내었다. Intersil ODS-3 C18(4.6 × 250 mm, 5.0 µm)의 peak 머무름 시간이 8.3분으로 Shiseido Capcell Pak C18 UG 120 (4.6 × 250 mm, 5.0 µm) 컬럼의 6.2분에 비해 늦게 나타났고, 피크 모양이 불량인 spike peak가 확인되어 peak가 보다 빨리 검출되고 정상적인 피크 모양이 확인된 Shiseido사의 컬럼을 선택하였다(Fig. 1). Spectrophotometer를 사용하여 200 nm부터 400 nm까지의 흡수파장을 분석한 결과 pectolinarin의 최대흡수파장을 340 nm로 하여 분석하였다. Jeong et al. (2013)에 의하면 pectolinarin 및 pectolinarigenin을 332 nm에서 분석하였다고 보고하여 본 연구의 결과와 유사한 경향을 나타내었다.
Table 1.
HPLC conditions for pectolinarin analysis
| Analytical condition | |||
| Column temp. | 40°C | ||
| HPLC | Waters 2695 HPLC system | ||
| Detector | Waters 996 PDA Detector (340 nm) | ||
| Column | Shiseido Capcell Pak C18 UG 120 (4.6 × 250 mm, 5.0 µm) | ||
| Mobile phase | Time (min) | A1) | B2) |
| 0 | 70 | 30 | |
| 6 | 70 | 30 | |
| 11 | 53 | 47 | |
| 22 | 53 | 47 | |
| 25 | 70 | 30 | |
| 30 | 70 | 30 | |
| Injection vol. | 10 µL | ||
| Flow rate | 1.0 mL/min | ||
특이성 확인
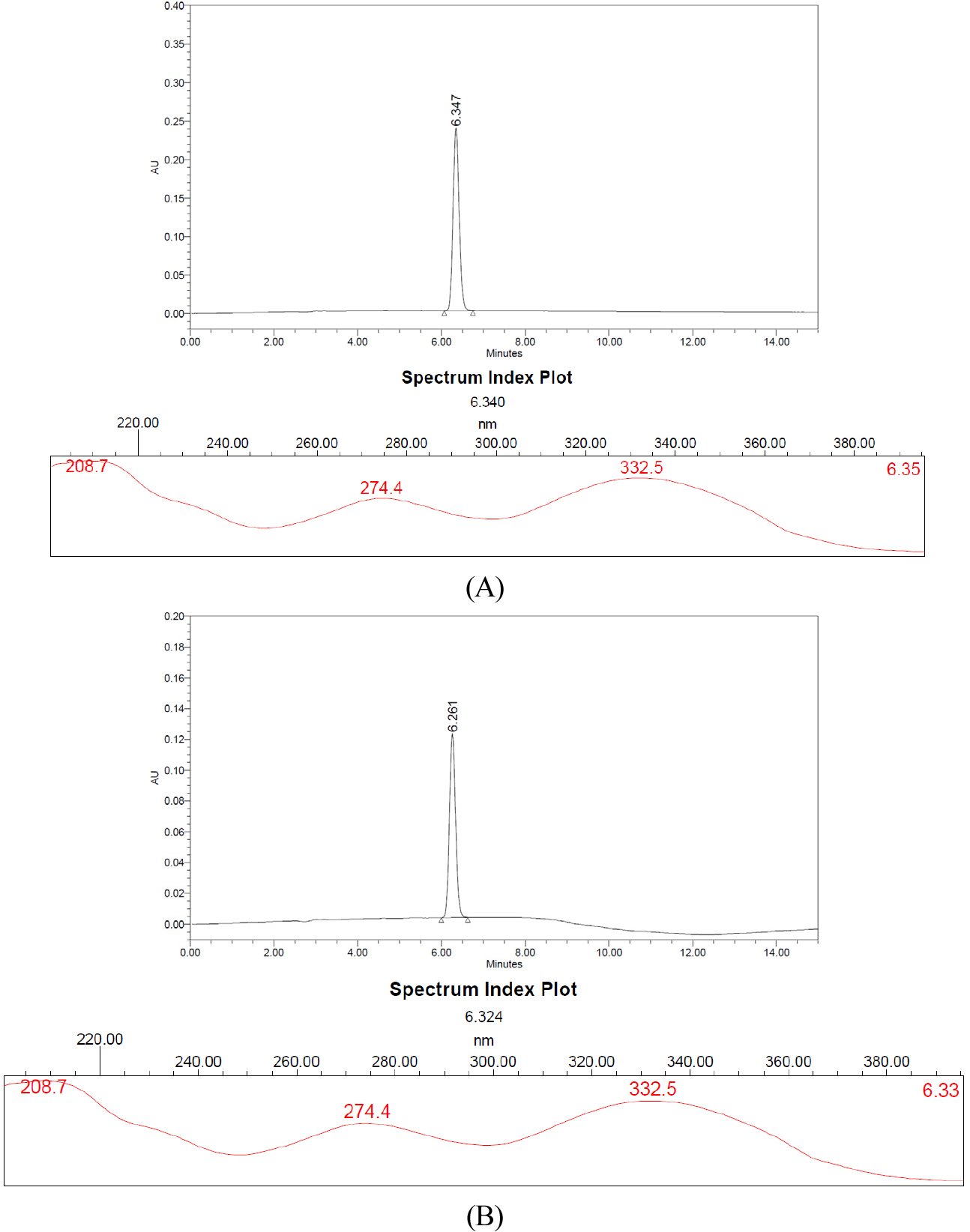
불순물, 분해물, 배합성분 등의 혼재 상태에서 분석대상물질을 선택적으로 측정할 수 있는 능력인 특이성은 다른 물질의 간섭 없이 peak가 분리되는 것으로 특이성을 확인할 수 있다. HPLC-PDA를 이용하여 pectolinarin 표준물질과 시료의 chromatogram과 spectrum을 비교한 결과는 Fig. 2에 나타내었다. 시료와 표준물질의 머무름 시간(retention time, RT)이 일치하는 것을 확인하였고, UV spectrum 결과도 동일한 스펙트럼을 나타내었으며 동일한 지표물질이 곤드레 분말 샘플 내의 다른 성분들로부터 간섭을 받지 않고 특이적으로 확인되었음을 확인하였다.
직선성 확인
직선성은 시료 중 일정 범위 내에서 분석대상물질의 양에 비례하는 직선적인 측정값을 얻어낼 수 있는 능력을 말하며, 분석된 결과에 따라 y축을 peak 면적, x축을 표준용액의 농도(µg/mL)로 하여 작성된 calibration curve의 R2값으로 직선성을 확인하였다. Pectolinarin 표준물질의 최종농도가 0.5, 1, 5, 10, 25, 50, 100 µg/mL가 되도록 희석한 후 HPLC-PDA로 분석하여 직선성을 살펴본 결과는 Table 2에 나타난 결과와 같다. 검량선의 결정계수인 R2값이 0.9979로 양호한 값을 나타내는 것을 확인하였다(Fig. 3).
Table 2.
Correlation coefficients of the calibration curves and limits of detection (LOD) and quantification (LOQ) of pectolinarin for standardized Cirsium setidens fine powder by air-classification
| Analytes | Range (µg/mL) | Slope | Intercept | Correlation coefficient (R2) | LOD (µg/mL) | LOQ (µg/mL) |
| Pectolinarin | 0.5-100 | 23481 | 51776.86 | 0.9979 | 0.11 | 0.34 |
정밀성 및 정확성
정밀성은 균일한 시료에 대하여 연속적인 분석을 통해 얻은 각각의 측정값들 사이의 근접성을 의미하며, 정확성은 측정값이 이미 알고 있는 참값이나 표준값에 근접한 정도를 의미한다. 농도를 알고 있는 곤드레 분말 시료에 표준용액 pectolinarin을 10, 25, 50 µg/mL의 농도씩 각각 첨가하여 HPLC-PDA로 정밀성 및 정확성을 나타는 결과는 Table 3에 나타난 결과와 같다. Pectolinarin의 일내 및 일간 정밀성의 값은 0.28-2.35%로 ICH 가이드라인(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceutical for Human Use)에서 유의미한 결과로 제시한 5% 이내로 확인되었으며, 일내 및 일간 정확성의 값은 90.20-115.62%, 90.63-113.05% 수준으로 ICH 가이드라인에서 제시한 80-120% 이내의 결과로 확인하였다.
Table 3.
Recovery of pectolinarin from sample spiked at three different concentration (n = 3)
| Analytes | Concentration (µg/mL) | Mean ± SD (µg/mL) | RSD1) (%) | Recovery (%) |
| Intra- day | 10 | 11.56 ± 0.03 | 0.28 | 115.62 |
| 25 | 22.55 ± 0.37 | 1.64 | 90.20 | |
| 50 | 49.34 ± 0.17 | 0.35 | 98.68 | |
| Inter- day | 10 | 11.30 ± 0.23 | 2.35 | 113.05 |
| 25 | 22.66 ± 0.36 | 1.45 | 90.63 | |
| 50 | 49.59 ± 0.25 | 0.50 | 99.19 |
검출한계 및 정량한계
검량선의 기울기와 반응의 표준편차에 근거하는 방법을 사용하여 검출한계(LOD)와 정량한계(LOQ)를 구한 결과는 Table 2에 나타난 결과와 같다. 검출한계는 0.11 µg/mL, 정량한계는 0.34 µg/mL 수준으로 우수한 검출한계와 정량한계를 확인하였다. 이상의 결과를 종합하여 볼 때 미세분말 곤드레의 pectolinarin은 HPLC를 이용한 동시분석과 정량분석이 가능한 것으로 나타났다.
미세분말 공기분급을 통한 곤드레의 pectolinarin함량 분석
HPLC-PDA를 이용하여 곤드레 분말 샘플의 pectolinarin 함량을 분석한 결과는 Table 4와 같다. 미세분말 공기분급 곤드레 분말의 지표성분 함량은 11.07 ± 0.05 mg/g을 보였으며 조분쇄된 곤드레 분말(4.24 ± 0.02 mg/g)에 비해 pectolinarin의 함량은 2.61배 증가한 것으로 나타났다. 미세분말 공기분급 곤드레의 pectolinarin을 유용성분 및 지표성분으로 선정 시 분석법 검증을 통한 원료 표준화가 가능할 것으로 사료되며, 추출물 내 특이성을 보완하기 위해 HPLC-MS/MS 분석을 통한 추가 연구가 진행되어야 할 것으로 보인다.
요 약
본 연구에서는 HPLC를 이용하여 미세분말 공기분급 곤드레 분말의 pectolinarin의 분석법 검증을 실시하였다. 분석법은 특이성, 직선성, 정확성, 정밀성, 검출한계 및 정량한계를 통하여 신뢰성을 검증하였다. HPLC를 이용한 분석방법에서 표준용액과 공기분급 곤드레 분말의 머무름 시간이 일치하는 것을 확인하였다. 표준물질과 시료에서의 peak는 다른 성분의 간섭 없이 선택적으로 분리되는 것을 확인하다. Pectolinarin의 검량선은 상관계수 값이 각각 0.9979로 나타나 우수한 직선성을 나타내어 분석에 적합함을 확인하였다. Pectolinarin의 정밀성은 일간 정밀성과 일내 정밀성으로 확인하였으며, pectolinarin의 일내 및 일간 정밀성의 값은 0.28-2.35%로 5% 이하의 값을 나타내어 우수한 정밀성을 보였다. 정확성 측정 결과 pectolinarin의 일내 및 일간 정확성의 값은 90.20-115.62%, 90.63-113.05% 수준으로 우수한 정확성을 나타내었다. Pectolinarin의 검출한계는 0.11 µg/mL로 측정되었고, 정량한계는 0.34 µg/mL로 나타나 우수한 검출한계와 정량한계를 확인하였다. 미세분말 공기분급 곤드레 분말 시료 중 pectolinarin의 함량을 분석한 결과 11.07 mg/g의 함량을 가지고 있는 것으로 분석되었다. 분석법 검증 결과, 확립된 분석법은 직선성, 정밀성, 정확성, 검출한계 및 정량한계가 우수한 분석법임을 검증하였으나, 분석법의 특이성을 보완하고 검증된 분석법의 신뢰성을 확보하기 위하여 추후 LC-MS/MS 분석을 통한 추가 실험이 필요할 것으로 사료된다.